ليبوزوم
| د.لمى أورفه لي |
| المساهمة الرئيسية في هذا المقال |
جسيم شحمي الليبوزوم Liposome
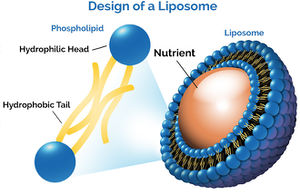
الجسيمات الشحمية هي عبارة عن حويصلات اصطناعية صغيرة ذات شكل كروي والتي يمكن أن تصنع من الكوليسترول و الفوسفوليبيدات الطبيعية الغير سامة
تتراوح أحجامها بين 30 نانومتر إلى عدة ميكرومترات وتتكون من واحدة أو أكثر من طبقات ثنائية الدهون تحيط بالوحدات المائية حيث يتم توجيه مجموعات الرؤوس القطبية إلى داخل أو خارج الأطوار المائية
و نظراً لحجمها و خصائصها الكارهة والمحبة للماء فإنها تعد أنظمة واعدة لتوصيل المواد الدوائية
تختلف الجسيمات الشحمية بشكل كبير مع الدهون من حيث الخصائص و شحنة السطح والحجم وطريقة التحضير
بالإضافة إلى ذلك فإن مكونات الطبقة الثنائية تحدد الصلابة أو السيولة و تحدد شحنة هذه الطبقة
فمثلًا تعطي مادة الفوسفاتيديل كولين غير المشبعة المستخرجة من المصادر الطبيعية كالبيض أو فول الصويا طبقات ثنائية أكثر قدرة على النفاذية وأقل استقرارًا في حين أن الفوسفوليبيدات المشبعة ذات سلاسل الأسيل الطويلة تشكل بنية ثنائية الطبقة صلبة وغير منفذة إلى حد ما
وقد تبين أن الفوسفولبيدات تشكل هياكل مغلقة في الأوساط المائية لذا فإن الحويصلات التي تحتوي على غشاء أو أكثر من الفوسفولبيدات ثنائية الطبقة تنقل الأدوية المائية أو الدهنية اعتمادًا على طبيعة تلك الأدوية
الاستخدامات
تستخدم الجسيمات الشحمية على نطاق واسع كحامل للجزيئات المحبة للماء أو الكارهة للماء و ذلك في مجال صناعات التجميل و الصناعات الدوائية كما تم دراسة استخدامها في مجال الصناعات الغذائية والزراعية لتطوير نظم إيصال المركبات الغير مستقرة مثل مضادات الأحياء الدقيقة و مضادات الأكسدة و النكهات و العناصر النشطة حيويًا حيث تحمل الجسيمات الشحمية هذه المواد داخلها و تحميها لتقوم بوظائفها
و بسبب التوافق الحيوي للجسيمات الشحمية و قابليتها للتحلل الحيوي و انخفاض سميتها و قدرتها على توصيل الأدوية إلى مواقعها المحددة زاد استخدامها بشكل كبير في السنوات الأخيرة
تصنيف الجسيمات الشحمية
تصنف الجسيمات الشحمية حسب حجمها و عدد الطبقات التي تتألف منها حيث يتراوح حجم الجسيمات الشحمية بين 0.025 ميكرومتر و 2.5 ميكرومتر
و قد تحتوي على واحد أو أكثر من الأغشية ثنائية الطبقة
يحدد حجم الحويصلة نصف عمر دورة حياة الجسيمات الشحمية و يؤثر كل من الحجم وعدد الطبقات على كمية الدواء المغلف داخل الجسيمات الشحمية
يمكن أيضًا تصنيف الجسيمات الشحمية إلى فئتين
الحويصلات متعددة الصفيحات و الحويصلات وحيدة الصفيحات حيث يكون غشائها ذو الطبقة الفوسفولبيدية الثنائية محيط بالمحلول المائي
و تصنف الحويصلات وحيدة الصفيحات إلى فئتين حويصلات كبيرة (LUV) و حويصلات صغيرة (SUV)
طرق تحضير الجسيمات الشحمية
تتضمن كل طرق تحضير الجسيمات الشحمية أربع مراحل أساسية
- تجفيف الدهون من المذيبات العضوية
- توزيع الدهون في الوسط المائي
- تنقية الجسيمات الناتجة
- تحليل المنتج النهائي
و تتضمن طرق التحضير و تحميل الدواء:
- تقنيات التحميل السلبية
- تقنية التحميل النشطة
تتضمن تقنيات التحميل السلبي ثلاث طرق مختلفة:
- طريقة التشتت الميكانيكية
- طريقة التشتيت بالمذيبات
- طريقة إزالة المنظفات (إزالة المواد غير المغلفة)
طريقة التشتت الميكانيكي
وتتضمن:
الصوتنة Sonication
هذه الطريقة هي الأكثر استخدامًا لإعداد الحويصلات الصغيرة وحيدة الصفيحة و تتمثل العيوب الرئيسية لهذه الطريقة في انخفاض كفاءة التغليف الداخلي و التدهور المحتمل للفوسفوليبيدات والمركبات المراد تغليفها و احتمال التلوث المعدني من الأدوات المستخدمة و ظهور الحويصلات المتعددة الطبقة مع الحويصلات الصغيرة الناتجة
خلية الضغط الفرنسية (القذف)
و تستخدم لتحضير الحويصلات متعددة الطبقات ولها عدة مميزات عن الطريقة السابقة:
- تجميد الجسيمات الشحمية بسرعة و تذويبها ببطء
- ترطيب الفيلم الدهني
- الاستحلاب الدقيق
- قذف الغشاء
- إعادة التشكيل الجاف
طريقة التشتيت بالمذيبات
وتتضمن:
- حقن الإيتر (تبخير المذيب) :
حيث يتم حقن محلول من الدهون المذابة في خليط ثنائي إيتيل الإيتر أو مزيج الإيتر والميتانول تدريجياً إلى محلول مائي من المادة المراد تغليفها و ذلك عند درجة حرارة 55 / 65 درجة مئوية و تحت ضغط مخفض و يؤدي تبخير الإيتر في هذه الظروف إلى تكوين الجسيمات الشحمية
تتمثل المساوئ الرئيسية لهذه التقنية في تكوين جسيمات غير متجانسة الأحجام (من 70 إلى 200 نانومتر) بالإضافة إلى تعرض المواد لدرجات حرارة عالية
حقن الإيتانول
يتم حقن محلول الدهون المذاب في الإيتانول بسرعة إلى كمية كبيرة من محلول عازل مما يؤدي إلى تشكيل حويصلات متعددة الطبقات أيضًا عيوب هذه الطريقة هي أن حجم الحويصلات غير متجانس (30 إلى 110 نانومتر) بالإضافة إلى صعوبة إزالة جميع الإيتانول حيث يشكل خليط غازي ( إيزوتروبي ) مع الماء
طريقة التبخير العكسي
قدمت هذه الطريقة تقدمًا كبيرًا في تصنيع الجسيمات الشحمية و ذلك بطريقة يتواجد فيها حجم مائي عالي مقارنة مع نسبة الدهون و قد حققت نسبة احتواء كبيرة من المادة المائية الموجودة
العيب الرئيسي لهذه التقنية هو اتصال المواد المراد تغليفها بالمذيبات العضوية و تعرضها لفترة قصيرة من الصوتنة مما يؤدي في هذه الظروف إلى تكسر جزيئات حمض DNA و تمسخ بعض البروتينات أما الميزة الرئيسية لهذه الطريقة هي أن الجسيمات الشحمية لها كفاءة تغليف عالية (حوالي 80٪)
على الرغم من أن الجسيمات الشحمية تشبه الأغشية الحيوية إلا أنها تبقى أجسام غريبة في الجسم ولذلك تقوم الخلايا البلعمية أحادية النواة بالتعرف عليها لتقوم بتصفيتها من الدم
وقد تم حل هذه المشكلة من خلال :
- استخدام فوسفولبيدات اصطناعية
- استخدام جزيئات مغلفة مع البولي ايتيلين غليكول حيث يؤدي التغليف مع البولي ايتيلين غليكول على تقليل نسبة البلعمة من قبل الخلايا البالعة و إطالة زمن وجود الجسيمات الشحمية في الدورة الدموية و بالتالي توفير الوقت الكافي لهذه الجسيمات الشحمية لتقوم بعملها
- تغليف الجسيمات الشحمية مع مشتقات الكيتين
- التجفيف بالتجميد
- البلمرة
تحميل المواد الدوائية في الجسيمات الشحمية
يمكن تحميل الدواء إما بشكل سلبي أي أن الدواء يغلف أثناء تكوين الجسيمات الشحمية أو بطريقة نشطة أي بعد تكوين الجسيمات الشحمية
فالأدوية المحبة للماء مثلًا يتم تحميلها بشكل مباشر في الجسيمات الشحمية أثناء تكوين الحويصلات
أما بالنسبة للمواد الطبيعية فإنها تُحمل في الجسيمات الشحمية عبر تقنية التجفيف بالتجميد( التجفيد) و ذلك لأنها عادة ما تتحلل بسهولة عبر التفاعلات الكيميائية مثل الأكسدة قبل تسليمها إلى الموقع المستهدف
و تعتمد هذه التقنية إزالة الماء من المنتجات في حالة التجميد عند ضغوط منخفضة للغاية و تستخدم هذه العملية لتجفيف المواد التي تتخرب في حال تم تجفيفها بالحرارة و قد أثبتت هذه الطريقة فعالية عالية لثبات الجسيمات الشحمية و زيادة القدرة على الاحتفاظ بالمواد الدوائية داخلها
آلية نقل الدواء من خلال الجسيمات الشحمية
إن التفاعل بين الجسيمات الشحمية و الخلايا يتم عبر ما يلي
- امتزاز بسيط عبر تفاعلات محددة مع مكونات سطح الخلية
- ال[[بلعمة]ي عبر الخلايا البلعمية في الجهاز الشبكي
- الاندماج مع الغشاء البلاسمي الخلية عن طريق إدخال الطبقة ثنائية الدهون من الجسيمات الشحمية في غشاء البلاسما و إطلاق محتوى الجسيمات لكنه تفاعل نادر
تبادل مكونات الطبقة الثنائية مثل الكولسترول والدهون والجزيئات المرتبطة بغشاء الجسيمات مع مكونات أغشية الخلايا
تطبيقات الجسيمات الشحمية في الطب والصيدلة
يمكن تقسيم تطبيقات الجسيمات الشحمية في الطب والصيدلة إلى تطبيقات تشخيصية وعلاجية حسب المادة الدوائية التي تحملها
كما يمكن استخدامها كأداة أو كاشف في الدراسات الأساسية للتفاعلات الخلوية وطريقة عمل بعض المواد
و تستخدم أيضاً في الأدوية التي لديها نافذة علاجية ضيقة حيث يكون التركيز العلاجي قريب جدًا لتركيز السمية و هنا يمكن تقليل السمية أو تعزيز الفعالية عن طريق استخدام حاملة دواء مناسبة تعمل على تغيير التسليم الزماني والمكاني للدواء أي التوزيع الحيوي للدواء
فمثلًا ممكن تقليل سمية الأدوية المضادة للورم و الاحتفاظ بفعاليتها عندما تحمل من قبل الجسيمات الشحمية
أمثلة على التطبيقات
الجسيمات الشحمية في الأمراض الطفيلية والالتهابات
باعتبار أن الخلايا البلعمية تقوم ببلعمة الجسيمات الشحمية عند وصولها إلى الدورة الدموية فإن هذه الجسيمات هي حاملات دواء مثالية لتوصيل الدواء إلى هذه البلعميات و ذلك في حالة الأمراض الطفيلية التي تتواجد عادة في هذه الخلايا
و مثال على ذلك داء الليشمانيات حيث يستهدف الطفيلي الخلايا البلعمية و عند استخدام الجسيمات الشحمية لحمل دواء الأنتيمون تتراكم في مجموعة الخلايا المصابة و قد تم تسجيل حالات شفاء من المرض لكن بقيت هذه التجارب على حيوانات التجربة فقط و حديثًا أجريت تجارب جديدة لحمل مادة الأمفوتريسين B المفضل لعلاج الأمراض الفطرية و قد أظهر حمل هذا الدواء في الجسيمات الشحمية تثبيط تراكم الدواء في الأعضاء و التقليل من السمية بشكل جذري
يمكن تحقيق طرق مماثلة في العلاجات المضادة للفيروسات والمضادة للجراثيم و ذلك للأدوية التي تكون عادةً شديدة السمية بطريق الحقن لكن تقديم المضادات الحيوية بهذه الطريقة لا يعتبر سهلًا لصعوبة التحضير وتفاعل هذه المواد مع الطبقة الفوسفولبيدية و تجرى حاليًا العديد من الأبحاث لتسهيل تقديم الأدوية المضادة للجراثيم و المضادة للفيروسات عبر الجسيمات الشحمية
الجسيمات الشحمية في العلاج المضاد للسرطان
إن العديد من الجسيمات الشحمية الحاملة للعوامل المضادة للسرطان أقل سمية من الدواء وحده
فالأنثراسيكلينات التي توقف نمو الخلايا المنقسمة عن طريق إقحامها في الحمض النووي DNA تقتل الخلايا التي تنقسم بسرعة كبيرة لكنها في الوقت نفسه تقتل الخلايا التي تنقسم أيضًا في الجسم كالشعر و الغشاء المخاطي المعوي و خلايا الدم بالإضافة أن جرعتها محدودة بسبب سميتها على القلب
لكن عند تقديم هذه الأدوية عبر الجسيمات الشحمية فإن السمية تنخفض إلى حوالي 50 ٪