الفرق بين المراجعتين لصفحة: «كلوريد الصوديوم»
كنان الطرح (نقاش | مساهمات) لا ملخص تعديل |
كنان الطرح (نقاش | مساهمات) لا ملخص تعديل |
||
| سطر 112: | سطر 112: | ||
https://en.wikipedia.org/wiki/Sodium_Chloride | https://en.wikipedia.org/wiki/Sodium_Chloride | ||
{{ثبت المراجع}} | |||
{{مكملات معادن}} | {{مكملات معادن}} | ||
[[تصنيف:أدوية]] | [[تصنيف:أدوية]] | ||
[[تصنيف:موسوعة الأدوية]] | [[تصنيف:موسوعة الأدوية]] | ||
[[تصنيف:مكملات معادن]] | [[تصنيف:مكملات معادن]] | ||
المراجعة الحالية بتاريخ 16:23، 13 أكتوبر 2013
| كلوريد الصوديوم | |
|---|---|

|

|

|

|
Sodium chloride | |
Other names Common salt Halite | |
| المعرفات | |
| رقم CAS | |
| بوبكيم (PubChem) | |
| ChemSpider | 5044 |
| UNII | 451W47IQ8X |
| EC number | 231-598-3 |
| KEGG | D02056 |
| MeSH | |
| ChEBI | CHEBI:26710 |
| ChEMBL | CHEMBL1200574 |
| RTECS number | VZ4725000 |
| كود ATC | A12,B05CB01, B05XA03 |
| Beilstein Reference | 3534976 |
| Gmelin Reference | 13673 |
| Jmol-3D images | Image 1 |
| |
| |
| الخصائص | |
| صيغة جزيئية | NaCl |
| الكتلة المولية | 58.44 g mol−1 |
| المظهر | Colorless crystals |
| Odor | Odorless |
| الكثافة | 2.165 g cm−3 |
| نقطة الانصهار |
801 °C, 1074 K, 1474 °F |
| نقطة الغليان |
1413 °C, 1686 K, 2575 °F |
| قابلية الذوبان في الماء | 359 g L−1 |
| قابلية الذوبان في ammonia | 21.5 g L−1 |
| قابلية الذوبان في methanol | 14.9 g L−1 |
| Refractive index (nD) | 1.5442 (at 589 nm) |
| Structure | |
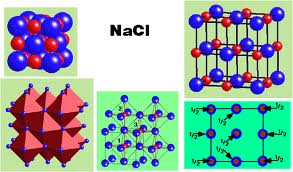
| Crystal structure | Cubic (see text), cF8 |
| Space group | Fm3m, No. 225 |
| Lattice constant | a = 564.02 pm |
| Coordination geometry |
Octahedral (Na+) Octahedral (Cl−) |
| Thermochemistry | |
| Std enthalpy of formation ΔfH |
−411.12 kJ mol−1 |
| Standard molar entropy S |
72.11 J K−1 mol−1 |
| Specific heat capacity, C | 36.79 J K−1 mol−1 |
| المخاطر | |
| NFPA 704 | |
| LD50 | 3000–8000 mg/kg (oral in rats, mice, rabbits)[1] |
| مركبات قريبة | |
| Other anions | Sodium fluoride Sodium bromide Sodium iodide |
| Other cations | Lithium chloride Potassium chloride Rubidium chloride Caesium chloride |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
كلور الصوديوم Sodium Chloride
الصيغة الكيميائية
الوصف Characters
مسحوق بلوري أبيض، أو بلورات عديمة اللون، أو بيضاء لؤلؤية، تنحل بحرية في الماء، غير منحل عملياً الكحول الخالي من الماء.
الاستعمال Use
عامل ممدد diluent للكبسولات والمضغوطات، وعامل للتوتر السطحي tonicity agent.
التنافرات Incompatibilities
المحاليل المائية لكلور الصوديوم تكون آكالة للحديد، كما أنها تتفاعل وتشكل رواسب مع أملاح الفضة والرصاص والزئبق، العوامل المؤكسدة القوية تحرر الكلور من المحاليل المحمضة لكلور الصوديوم. إن انحلال بعض المواد الحافظة الميكروبية ينقص في محاليل كلور الصوديوم. كما أن لزوجة هلام الكربومير، ومحاليل هيدروكسي ايتيل السيللوز، أو هيدروكسي بروبيل السيللوز، تنقص بإضافة كلور الصوديوم.
الحفظ والتخزين Packaging and Storage
إن المادة الصلبة ثابتة، ويجب حفظها في عبوات محكمة الإغلاق، في أماكن باردة وجافة.
المصادر
دساتير الأدوية.
https://en.wikipedia.org/wiki/Sodium_Chloride
- ↑ Martel, B.; Cassidy, K. (2004). Chemical Risk Analysis: A Practical Handbook. Butterworth–Heinemann. p. 369. ISBN 1-903996-65-1.