الفرق بين المراجعتين لصفحة: «بايبيريدين»
اذهب إلى التنقل
اذهب إلى البحث
كنان الطرح (نقاش | مساهمات) (أنشأ الصفحة ب'{{chembox | English = Piperidine | verifiedrevid = 464207528 | References=<ref>[http://www.ilo.org/public/english/protection/safework/cis/products/icsc/dtasht/_icsc03/...') |
كنان الطرح (نقاش | مساهمات) لا ملخص تعديل |
||
| (مراجعتان متوسطتان بواسطة نفس المستخدم غير معروضتين) | |||
| سطر 51: | سطر 51: | ||
| NFPA-F = 3 | | NFPA-F = 3 | ||
| NFPA-R = 3 | | NFPA-R = 3 | ||
| RPhrases = {{R11}}, {{R23/24}}, {{R34}} | | RPhrases = {{R11}}, {{R23/24}}, {{R34}} | ||
}} | }} | ||
| سطر 58: | سطر 57: | ||
}} | }} | ||
}} | }} | ||
'''بايبيريدين (Piperidine)''' | '''بايبيريدين (Piperidine)''' مركب عضوي له الصيغة C5H5N وهو من المركبات العطرية الحلقية غير المتجانسة. بنية البيريدين تتكون من حلقة سداسية غير مشبعة حاوية على ذرة نيتروجين. | ||
==الاستعمال== | |||
*يستخدم البيريدين بكثرة في الاصطناع العضوي كمحل (مذيب) وكمادة متفاعلة. | |||
*يدخل البيريدين في صناعة العديد من الصناعات الكيميائية مثل الصناعات الدوائية، وصناعة المبيدات الحشرية والعشبية، وصناعة المطاط واللواصق. | |||
==الخواص الكيميائية== | |||
*البيريدين سائل عديم اللون، له رائحة كريهة. | |||
*يمتزج البيريدين مع الماء، كما أنه يمتزج مع أغلب المحلات العضوية مثل الإيثانول والكلوروفورم وثنائي إيثيل الإيثر والأسيتون. | |||
*يعد البيريدين من الحلقات العطرية القاعدية، حيث يتفاعل البيريدين مع الأحماض القوية مثل حمض كلور الماء مشكلاً ملح هيدرو الكلوريد الذي ينصهر عند 145°س. | |||
*نتيجة وجود ذرة النيتروجين الكهرسلبية (الساحبة للإلكترونات) فإن الحلقة البيريدينية فقيرة بالإلكترونات نسبياً، مما يثبط بالتالي حدوث تفاعلات الاستبدال المحبة للإلكترونات (الاستبدال الإلكتروفيلي) النمطية للمركبات العطرية. | |||
==التحضير== | |||
يوجد البيريدين طبيعياً في قطران الفحم. كما يمكن اصطناع البيريدين من الأسيت ألدهيد والفورمالدهيد والأمونياك. تدعى هذه العملية اصطناع تشيتشيبابين للبيريدين. | |||
CH2O + NH3 + 2 CH3CHO → C5H5N + 3 H2O + H2 | |||
==المصادر== | |||
https://en.wikipedia.org/wiki/Pyridine | |||
{{ثبت المراجع}} | |||
{{حاصرات قنوات الكالسيوم}} | {{حاصرات قنوات الكالسيوم}} | ||
[[تصنيف:أدوية]] | [[تصنيف:أدوية]] | ||
المراجعة الحالية بتاريخ 06:36، 30 يونيو 2013
| Piperidine | |
|---|---|
|

|

| |
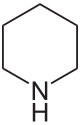
Piperidine | |
Other names Hexahydropyridine | |
| المعرفات | |
| رقم CAS | |
| بوبكيم (PubChem) | |
| ChemSpider | 7791 |
| UNII | 67I85E138Y |
| ChEBI | CHEBI:18049 |
| ChEMBL | CHEMBL15487 |
| RTECS number | TM3500000 |
| Jmol-3D images | Image 1 |
| |
| |
| الخصائص | |
| الصيغة الجزيئية | C5H11N |
| كتلة مولية | 85.15 g mol-1 |
| المظهر | colourless liquid |
| الكثافة | 0.862 g/mL, liquid |
| نقطة الانصهار |
−7 °C, 266 K, 19 °F |
| نقطة الغليان |
106 °C, 379 K, 223 °F |
| قابلية الذوبان في الماء | miscible |
| الحموضة (pKa) | 11.22[1] |
| اللزوجة | 1.573 cP at 25 °C |
| المخاطر | |
| R-phrases | R11, R23/24, R34 |
| NFPA 704 | |
| مركبات قريبة | |
| Related compounds | pyridine pyrrolidine piperazine |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
بايبيريدين (Piperidine) مركب عضوي له الصيغة C5H5N وهو من المركبات العطرية الحلقية غير المتجانسة. بنية البيريدين تتكون من حلقة سداسية غير مشبعة حاوية على ذرة نيتروجين.
الاستعمال
- يستخدم البيريدين بكثرة في الاصطناع العضوي كمحل (مذيب) وكمادة متفاعلة.
- يدخل البيريدين في صناعة العديد من الصناعات الكيميائية مثل الصناعات الدوائية، وصناعة المبيدات الحشرية والعشبية، وصناعة المطاط واللواصق.
الخواص الكيميائية
- البيريدين سائل عديم اللون، له رائحة كريهة.
- يمتزج البيريدين مع الماء، كما أنه يمتزج مع أغلب المحلات العضوية مثل الإيثانول والكلوروفورم وثنائي إيثيل الإيثر والأسيتون.
- يعد البيريدين من الحلقات العطرية القاعدية، حيث يتفاعل البيريدين مع الأحماض القوية مثل حمض كلور الماء مشكلاً ملح هيدرو الكلوريد الذي ينصهر عند 145°س.
- نتيجة وجود ذرة النيتروجين الكهرسلبية (الساحبة للإلكترونات) فإن الحلقة البيريدينية فقيرة بالإلكترونات نسبياً، مما يثبط بالتالي حدوث تفاعلات الاستبدال المحبة للإلكترونات (الاستبدال الإلكتروفيلي) النمطية للمركبات العطرية.
التحضير
يوجد البيريدين طبيعياً في قطران الفحم. كما يمكن اصطناع البيريدين من الأسيت ألدهيد والفورمالدهيد والأمونياك. تدعى هذه العملية اصطناع تشيتشيبابين للبيريدين.
CH2O + NH3 + 2 CH3CHO → C5H5N + 3 H2O + H2
المصادر
https://en.wikipedia.org/wiki/Pyridine
- ↑ Hall, H.K., J. Am. Chem. Soc., 1957, 79, 5441.
