حمض الليمون
حمض الليمون Citric Acid يوجد بكثرة في العالم النباتي، تتراوح نسبته في عصير الليمون بين 5-7% ويوجد في الحليب وبكميات قليلة في الدم وبالعضلات والبول.
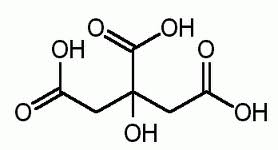
الصيغة الكيميائية
2-هدروكسي بروبان -1،2،3- تري كاربونيك
الحصول عليه
من عصير الليمون، بغليه ثم ترشيحه ومعالجة الرشاحة بكربونات الكالسيوم حيث يتحول الحمض إلى الملح الكلسي الذي يعالج بحمض الكبريت، كما يستحصل حيوياً باختمار الغلكوز أو قصب السكر أو النشا بتأثير بعض الفطور مثل Aspergillus - Citromyces وبمردود يتراوح بين 50-60% يعطي اختمار الغلكوز الهوائي جزئية من حمض الليمون وجزيئتين ماء.
الوصف
بلورات عديمة اللون، كثيرة الانحلال بالماء والإيثانول، يتبلور من محاليله المائية محتفظاً بجزيئة من ماء التبلور.
إذا سخن فوق الدرجة 175م فإنه يعطي حمض الأكونيت بعد خسارة جزيئة ماء.
الكشف
- تفاعل دينيجيس، بمعالجته بفوق منغنات البوتاسيوم بوجود HgSo4 والتسحين حتى الغليان فينتج حمض أسيتون دي كاربونيك الذي يتحد مع HgSo4 معطياً راسب أبيض عديم الانحلال بالماء.
- أكسدته في وسط حمضي بـKMno4 تعطي الأسيتون الذي يعطي مع ماء البروم راسب هو الكيتون خماسي البروم.
المقايسة
- مقياس الأسس بوجود مشعر الفينول فتالئين مع الأخذ بعين الاعتبار احتواؤه على 3 مجموعات كاربوكسيل، أو بالأكسدة حيث يتحول إلى الأسيتون الذي يقايس بمقياس اليود.
الاستعمال
لا يستعمل حراً في المداواة، ويقتصر ذلك على أخذه داخلاً بشكل شراب داخلاً أو خارجاً على شك قطرة عينية بتركيز 5% عنذ الوليدين للوقاية من التهاب الملتحمة.
أملاحه
المصدر
منشورات جامعة دمشق