الفرق بين المراجعتين لصفحة: «غليسرول»
(أنشأ الصفحة ب'{{Chembox new | Name =جليسرول Glycerol | ImageFile = Glycerine chemical structure.png <!-- | ImageSize = 200px --> | ImageName = Glycerol | ImageFile1 = Gly...') |
لا ملخص تعديل |
||
| سطر 106: | سطر 106: | ||
{{بذرة كيمياء}} | {{بذرة كيمياء}} | ||
[[تصنيف: صيدلة]] | |||
[[تصنيف:محليات]] | |||
[[تصنيف: | |||
[[تصنيف: | |||
[[تصنيف:مذيبات كحولية]] | [[تصنيف:مذيبات كحولية]] | ||
[[تصنيف:ملينات]] | [[تصنيف:ملينات]] | ||
[[تصنيف: | [[تصنيف: بوليميرات]] | ||
[[bg:Глицерин]] | [[bg:Глицерин]] | ||
مراجعة 21:06، 19 نوفمبر 2010
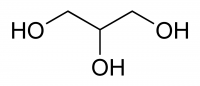
| جليسرول Glycerol | |
|---|---|
| |

| |

| |
Propane-1,2,3-triol | |
Other names glycerin | |
| المعرفات | |
| رقم CAS | |
| Jmol-3D images | Image 1 |
| |
| الخصائص | |
| صيغة جزيئية | C3H5(OH)3 |
| الكتلة المولية | 92.09382 g/mol |
| الكثافة | 1.261 g/cm³ |
| نقطة الانصهار |
18 °C (64.4°F) |
| نقطة الغليان |
290 °C (554°F) |
| اللزوجة | 1.5 Pa·s |
| المخاطر | |
| NFPA 704 | |
| Flash point | 160 °C (closed cup) |
| Except where noted otherwise, data are given for materials in their standard state (at 25 °C, 100 kPa) Infobox disclaimer and references | |
الگليسرول (بالإنجليزية: Glycerol) ويعرف أيضاً بأسماء جليسرين وجلسرن، وله أسماء أخرى غير مشهورة وهى بروبان-3،2،1-ترايول propane-1,2,3-triol و3،2،1 بروبانترايول 1,2,3-propanetriol، و3،2،1 ترايهيدروكسي بروبان 1,2,3-trihydroxypropane، وجلسريتول glyceritol، وأخيراً كحول جليسيل glycyl alcohol. وهو سائل لزج له طعم حلو، هيجروسكوبي، ليس له رائحة أو لون. الجليسرول هو كحول سكري وسبب ذوبانه في الماء هو وجود ثلاث مجاميع هيدروكسيل كحولية (-OH).
التصنيع
لما كان الگليسرول يشكل العمود الفقري للگليسريدات الثلاثية، فإنه يتم إنتاجها في عملية التصبن أو saponification. صناعة الصابون وانتاج الديزل الحيوي من خلال عملية transesterification هم أمثلة على تلك العمليات بالترتيب.
الاستخدامات
صيدلانياً
يستعمل الگليسرول كمادة حافظة ومادة مطرية ومرطبة وملدنة ومحلة ومحلية ورافعة للتوتر السطحي[1].
أيض الجليسرول
يحتوي الكبد على مخزون من الدهون المتعادلة والفسفورية ، كما أنه يستقبل بشكل دائم دهونا متعادلة من الغذاء ، ومن الدهون المخزنة في الجسم بهدف أكسدتها ، وسواء أكانت المادة التي أكدستها الكبد دهونا متعادلة أو فوسفورية ، فإن الجزء الأساسي في هذه العملية يتمثل في أكسدة الأحماض الدهنية طويلة السلسلة في الميتوكندريا. أما جزئ الجلسرين فيتفاعل مع جزي أدينوسين ثلاثي الفوسفات لإنتاج فوسفات الجلسرين التي تتم أكسدتها إلى جليرسيرالدهيد – 3 – فوسفات ، وهذا الجزئ إما أن يتحول إلى جليكوجين من خلال المسار العكسي لعملية تحلل الجلوكوز ، وإما أن يتحول إلى حمض البيرفيك.
وتتم أيضا أكسدة الأحماض الدهنية في العضلات ، ففي العضلات القلبية تمثل الأحماض الدهنية بالفعل مصدرا معما للطاقة و التنفس ، كما تؤكسد عضلة الحجاب الحاجز الأحماض الدهنية ، أما إذا وجد الجلوكوز فإن هذه العضلة تفضله على الأحماض الدهني. وطبقا لنظرية أكسدة الأحماض الدهنية من نوع بيتا ، فإن سلاسل الأحماض الدهنية تتم أكسدتها: للتخلص من ذرتي كربون في كل مرة ويتم ذلك بمهاجمة ذرة الكربون في الموقع بيتا بالنسبة إلى مجموعة الكربوكسيل بحيث يتحول الحمض الدهني إلى الحمض الكيتوني المقابل ، أما ذرتا الكربون الطرفيتنات فيتم التخلص منهما على هيئة حمض خليك ، ثم يتم عمل مجموعة كربوكسيل في موضع المجموعة الكيتونية ، وبذلك يتكون حمض دهني جديد ينقص عن الحمض الأصلي بمقدار ذرتي كربون ، ويلي ذلك مهاجمة ذرة كربون مرة أخرى في الموقع بيتا لتتكرر الخطوات السابقة ، وينتج حمض دهني جديد يقل ذرتي كربون عن الحمض الأصلي. وبهذه الطريقة يتم تكسير الحمض الدهني ، بإزالة ذرتي الكربون في كل مرة ينتج في المرحلة النهائية جزئ يسمى حمض الخليك الخللي ، الذي يسمى أيضا حمض بيتا – كيتوبيوتيريك. ولكي يتم أكسدة الاحماض الدهنية ، يلزم أولا تنشيطها عن طريق تكوين مشتقات المرافق الإنزيمي أ.
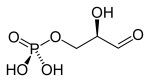
| Glycerol | Glycerol kinase | Glycerol-3-phosphate | Glycerol-3-phosphate dehydrogenase | Dihydroxyacetone phosphate | Triosephosphate isomerase | Glyceraldehyde 3-phosphate | |||
| ATP | ADP | NAD+ | NADH |
| |||||
|
|

| |||||||
| NAD+ | NADH |
||||||||
التنافرات
من الممكن أن ينفجر إذا مزج مع عوامل مؤكسدة قوية مثل ثلاثي أكسيد الكروميوم، وكلورات البوتاسيوم و برمنغنات البوتاسيوم، في المحاليل الممدة يحدث هذا التفاعل بشكل أبطأ مع تشكيل بعض نواتج الأكسدة، وتبدل لون الغليسيرن للأسود يكون نتيجة تعرضه للضوء أو أكسيد الزنك أو نترات البزموت الأساسية، كما أن احتواء الغليسرين على شوائب الحديد هي المسؤولة عن اللون الداكن لمزائجه مع الفينولات والصفصافات و التانين. يشكل الغليسرين معقد مع حمض البور (حمض غليسروبوريك) وهو حمض أقوى من حمض البور.
الحفظ
من الممكن أن يتبلور الگليسرول إذا حفظ في درجات الحرارة المنخفضة، ولا تذوب هذه البلورات إلا إذا تم تسخينها لدرجة 20 درجة مؤية من جديد، لذلك يجب أن يحفظ الغليسرين في عبوات محكمة الإغلاق، في أماكن رطبة وبدرجة حراة الغرفة.
المصادر
- Martindal
وصلات خارجية
- Glycerol on BioChemInfo.org
- Absolute alcohol using glycerol
- Computational Chemistry Wiki
- Physical Propetry of glycerol
bg:Глицерин cs:Glycerol da:Glycerin de:Glycerin en:Glycerol eo:Glicerino es:Glicerol fi:Glyseroli fr:Glycérol he:גליצרול hr:Glicerol is:Glýseról it:Glicerolo ja:グリセリン ko:글리세롤 lb:Glycerol lt:Glicerolis lv:Glicerīns nl:Glycerine nn:Glyserol no:Glyserol pl:Gliceryna pt:Glicerina ru:Глицерин sv:Propantriol zh:丙三醇
- ↑ Handbook of Pharmaceutical excipients

