الفرق بين المراجعتين لصفحة: «حالة سائلة»
ط (١ مراجعة: كيمياء) |
(لا فرق)
|
مراجعة 16:51، 13 نوفمبر 2010
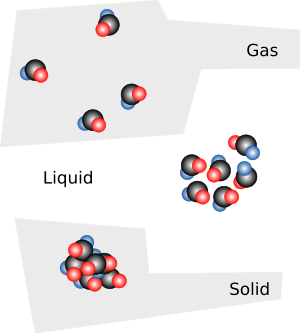
فيالفيزياء وفي الكيمياء الحالة السائلة احدي ثلاث حالات تهتم بهم الديناميكا الحرارية بجوار الحالة الغازية و الحالة الصلبة .
الديناميكا الحرارية تدرس انتقال المادة من الحالة السائلة إلى الحالة الغازية بالتسخين مثلا حيث يتحول الماء إلى الحالة الغازية أي إلى بخارز كذلك يمكن أن تنتقل المادة من الحالة السائلة إلى الحالة الصلبة بالتبريد . فيتصلب الماء ويصبح ثلجا .
تعتمد حالة المادة على الحرارة T والحجم V والضغط P. ويوضح الشكل المرافق انتقال المادة من حالة إلى حالة بتأثير تلك المتغيرات ، وقد اتخذنا هنا مثال الماء للتوضيح . يبين الخط الأخضر تغير درجة الانصهار بتغير الضغط. ويبين الخط الأزرق تغير نقطة غليان الماء تحت تأثير الضغط . كما يبين المنحنى الأحمر التسامي ، حيث ينتقل الماء من الحالة الصلبة مباشرة إلى بخار واعتماد ذلك على الحرارة .
تتقابل الثلاث منحنيات عند النقطة الثلاثية ، وتختلف تلك النقطة من مادة لأخرى . فالنقطة الثلاثية للكحول مثلا تتميز بثلاثة قيم للمتغيرات الحرارة ، والحجم ، والضغط .
مخطط الطور (منحنى حالات المادة)
في النقطة الثلاثية تتواجد الثلاثة حالات للماء في نفس الوقت : الحالة الصلبة ، والحالة السائلة ، والحالة الغازية. ويمثل الأخضر تواجد الحالتين الميء السائل والثلج . بارتفاع درجة الحرارة يجب أن نرفع الضغط لكي نحافظ على تواجد الحالتين في نفس الوقت ، وإلا يتحول(ينصهر) الثلج إلى ماء . ويمثل الخط الأزرق غليان الماء وتحوله إلى بخار. بارتفاع الضغط ترتفع درجة حرارة الغليان ، وطالما نتحرك على الخط الأزرق يكون لدينا حالتين في توازن ، أي ماء يغلى وفوقه بخار ساخن . ويمكننا الاستمرار في رفع الضغط ودرجة الحرارة حتي نصل إلى النقطة الحرجة (critical point) ، وعندها نصل إلى حالة لا يكون فيها الماء سائلا ولا بخارا ، بل هي حالة تجمع بين الاثنين في مخلوط مشبع عالي الضغط والحرارة. وتبلغ النقطة الحرجة للماء عند درجة حرارة 647 كلفن أو 374 درجة مئوية . ويصل الضغط عند تلك النقطة إلى 218 ضغط جوي .
تعمل محطات القوي لاستغلال الماء وبخاره في تلك الحالة لتوليد الطاقة الكهربائية بوساطة التوربينات . وكما نعرف من دورة كارنو ترتفع كفاءة الإنتاج بارتفاع درجة حرارة البخار (وتبلغ الكفاءة عند النقطة الحرجة 39 % ) . لذلك تبذل محطات التوليد مجهودات لتسخين تلك الحالة المائية البخارية لدرجات أعلى من 374 درجة مئوية ، لكي ترفع كفاءة تحويل الطاقة الحرارية إلى طاقة كهربائية ، ومن تلك المحطات ما تصل كفاءته 46 % .
حالات أخرى للمادة
بالإضافة إلى تلك الثلاثة حالات للمادة المعتادة في حياتنا اليومية ، تعرفنا في العصر الحديث على حالات جديدة للمادة لم تـُعرف من قبل . وتُشكل حالة البلازما (فيزياء) ، حالة المادة تحت درجات حرارة عالية جدا ، حيث تنفصل الإلكترونات عن الذرة . هذه حالة غير مألوفة تتصرف فيها الجسيمات المتأينة والإلكترونات بطريقة غريبة ، ولذلك تسمى البلازما. من تطبيقات البلازما محاولات ترويض الطاقة الهيدروجينية في الانصهار النووي .
كذلك حالة الميوعة الفائقة التي اكتشف عام 1904 عند تبريد غاز الهيليوم تحت درجة حرارة 17و2 كلفن. في حالة الميوعة الفائقة يتسلق السائل جدران الوعاء ويغطيه تماما من الداخل . وإذا وجد ثقب أعلى الوعاء خرج منها في حالته السائلة . كما أن السائل في هذه الحالة لا يدور عندما نقوم بتدوير الوعاء وتصل درجة لزوجته الصفر.
حالات جديدة للمادة نعرفها في النجوم النيوترونية ، والنجوم المسماة القزم الأبيض، حيث ينهار البناء الذري وتتجمع جميع أنوية الذرات مع بعضها مشكلة مادة تزيد كثافتها عن مئات الآلاف من كثافة المواد المعهودة .
أنظر أيضا
bg:Течност ca:Líquid cs:Kapalina cy:Hylif da:Væske de:Flüssigkeit el:Υγρό en:Liquid eo:Likvaĵo es:Líquido et:Vedelik fa:مایع fi:Neste fiu-vro:Vedelüs fr:Liquide gl:Líquido he:נוזל hr:Tekućine hu:Folyadék id:Cairan io:Liquido is:Vökvi it:Liquido ja:液体 ko:액체 ln:Bomái lt:Skystis lv:Šķidrums mk:Течност ml:ദ്രാവകം mr:द्रव ms:Cecair nds:Fletigkeit nl:Vloeistof nn:Væske no:Væske nov:Liquide pl:Ciecz pt:Líquido qu:Puriqlla ro:Lichid ru:Жидкость simple:Liquid sl:Kapljevina su:Cacai sv:Vätska sw:Kiowevu ta:நீர்மம் tg:Моеъ th:ของเหลว tr:Sıvı uk:Рідина ur:مائع zh:液体 zh-min-nan:E̍k-thé zh-yue:液體/Penkyamp