الفرق بين المراجعتين لصفحة: «تبخير فجائي»
ط (١ مراجعة: كيمياء) |
ط (مراجعة واحدة) |
||
| (مراجعة متوسطة واحدة بواسطة نفس المستخدم غير معروضة) | |||
| سطر 13: | سطر 13: | ||
عملية التبخر الفجائي لسائل بمفره تتصف بأن [[أنتروبية|أنتروبيتها]] ثابتة ولذلك يسمى التمدد الأدياباتيكي. وتستنبط المعادلة الأتية للتعبير عن حالة التوازن الحراري على طرفي صمام الخلخلة، وهي تستخدم لتعيين كمية السائل التي تتحول فوريا إلى بخار: | عملية التبخر الفجائي لسائل بمفره تتصف بأن [[أنتروبية|أنتروبيتها]] ثابتة ولذلك يسمى التمدد الأدياباتيكي. وتستنبط المعادلة الأتية للتعبير عن حالة التوازن الحراري على طرفي صمام الخلخلة، وهي تستخدم لتعيين كمية السائل التي تتحول فوريا إلى بخار: | ||
:'''''X = 100 (H<sub>u</sub><sup>L</sup> – H<sub>d</sub><sup>L</sup>) | :'''''X = 100 (H<sub>u</sub><sup>L</sup> – H<sub>d</sub><sup>L</sup>) ÷ (H<sub>d</sub><sup>V</sup> – H<sub>d</sub><sup>L</sup>)''''' | ||
:{| border="0" cellpadding="2" | :{| border="0" cellpadding="2" | ||
| سطر 26: | سطر 26: | ||
|align=left|= إنثالبي السائل الابتدائي عند [[درجة حرارة]] و[[الضغط]] الابتدائي [[جول]]/ [[كيلوجرام]] | |align=left|= إنثالبي السائل الابتدائي عند [[درجة حرارة]] و[[الضغط]] الابتدائي [[جول]]/ [[كيلوجرام]] | ||
|- | |- | ||
!align=right|''H<sub>d</sub><sup>V</sup>''<br> | !align=right|''H<sub>d</sub><sup>V</sup>''<br /> | ||
|align=left|= إنثالبي البخار المتمدد عند [[نقطة الغليان|درجة حرارة التشبع]] والضغط النهائي <br> جول/كيلوجرام | |align=left|= إنثالبي البخار المتمدد عند [[نقطة الغليان|درجة حرارة التشبع]] والضغط النهائي <br /> جول/كيلوجرام | ||
|- | |- | ||
!align=right|''H<sub>d</sub><sup>L</sup>''<br> | !align=right|''H<sub>d</sub><sup>L</sup>''<br /> | ||
|align=left|= إنثالبي السائل الباقي عند ضغط ودرجة حرارة التشبع للحالة النهائية <br> ، جول/كيلوجرام | |align=left|= إنثالبي السائل الباقي عند ضغط ودرجة حرارة التشبع للحالة النهائية <br /> ، جول/كيلوجرام | ||
|} | |} | ||
إذا لم تتوفر بيانات الإنثالبي اللازمة للمعادلة أعلاه، تستخدم المعادلة الآتية: | إذا لم تتوفر بيانات الإنثالبي اللازمة للمعادلة أعلاه، تستخدم المعادلة الآتية: | ||
:'''''X = 100 | :'''''X = 100 · c<sub>p</sub> (T<sub>u</sub> – T<sub>d</sub>) ÷ H<sub>v</sub>''''' | ||
:{| border="0" cellpadding="2" | :{| border="0" cellpadding="2" | ||
| سطر 54: | سطر 54: | ||
|align=left|= [[نقطة الغليان|درجة حرارة التشبع]] °C للسائل عند الضغط النهائي | |align=left|= [[نقطة الغليان|درجة حرارة التشبع]] °C للسائل عند الضغط النهائي | ||
|- | |- | ||
!align=right|''H<sub>v</sub>''<br> | !align=right|''H<sub>v</sub>''<br /> | ||
|align=left|= درجة حرارة التبخر للسائل عند الضغط ودرجة حرارة التشبع النهاية <br> جول/كيلوجرام | |align=left|= درجة حرارة التبخر للسائل عند الضغط ودرجة حرارة التشبع النهاية <br /> جول/كيلوجرام | ||
|} | |} | ||
| سطر 71: | سطر 71: | ||
==المراجع== | ==المراجع== | ||
{{ | {{مراجع}} | ||
{{التقطير}} | {{التقطير}} | ||
| سطر 77: | سطر 77: | ||
{{تصنيف كومنز|Distillation}} | {{تصنيف كومنز|Distillation}} | ||
[[تصنيف:إجراءات كيميائية]] | |||
[[تصنيف:تحريك الموائع]] | |||
[[تصنيف:تدفئة وتكييف]] | |||
[[تصنيف:ديناميكا حرارية]] | |||
[[تصنيف:تقطير]] | [[تصنيف:تقطير]] | ||
[[تصنيف:تقنيات مخبرية]] | [[تصنيف:تقنيات مخبرية]] | ||
| سطر 82: | سطر 86: | ||
[[تصنيف:هندسة كيميائية]] | [[تصنيف:هندسة كيميائية]] | ||
[[تصنيف:كيمياء]] | [[تصنيف:كيمياء]] | ||
المراجعة الحالية بتاريخ 14:17، 16 سبتمبر 2013
| هذا المقال أو المقطع ينقصه الاستشهاد بمصادر. الرجاء تحسين المقال بوضع مصادر مناسبة. أي معلومات غير موثقة يمكن التشكيك بها وإزالتها.(أغسطس_2010) |
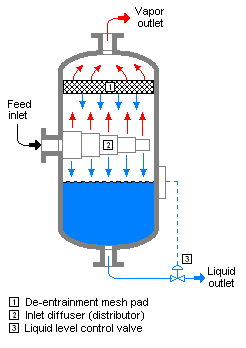
تبخير فجائي (بالإنجليزية:Flash evaporation) هي نشأة البخار فوق سائل مشبع عند نقطة الغليان عند خفض الضغط المفاجئ الذي يحدثة صمام تفريغ. وإذا كان الصمام مركبا عند مدخل خزان الضغط بحيث يحدث التفريغ المفاجئي وتكون البخار داخليا، فيسمى الخزان في هذه الحالة "خزان ضغط فجائي" أو خزان فصل السائل عن البخار.
وإذا كان السائل المشبع سائل نقي، مثل البروبان السائل أو الأمونيا السائلة، فيتمدد جزء من السائل فورا مكونا البخار. وتبدأ درجة حرارة البخار والسائل الباقي في الانخفاض إلى درجة حرارة التشبع للسائل عند ضغط منخفض. وتسمي تلك العملية تبريد مستمر وهي أساس عمل الثلاجات العادية التي تعمل بضغط البخار.
وإذا كان السائل مخلوط سوائل، مثل مخلوط البروبين والإيزوبوتان وبوتان عادي، يكون البخار المتكون غني ببخار السائل ذو تطاير نسبي عالي، وتقل نسبة هذا السائل في المخلوط المتبقي.
قد يؤدي التبخير الفجائي الغير متحكم فيه إلى غليان السائل وتمدده المفاجئ في صورة انفجار BLEVE.
التبخر الفجائي للسائل النقي
عملية التبخر الفجائي لسائل بمفره تتصف بأن أنتروبيتها ثابتة ولذلك يسمى التمدد الأدياباتيكي. وتستنبط المعادلة الأتية للتعبير عن حالة التوازن الحراري على طرفي صمام الخلخلة، وهي تستخدم لتعيين كمية السائل التي تتحول فوريا إلى بخار:
- X = 100 (HuL – HdL) ÷ (HdV – HdL)
حيث: X = نسبة الوزن المتبخرة HuL = إنثالبي السائل الابتدائي عند درجة حرارة والضغط الابتدائي جول/ كيلوجرام HdV
= إنثالبي البخار المتمدد عند درجة حرارة التشبع والضغط النهائي
جول/كيلوجرامHdL
= إنثالبي السائل الباقي عند ضغط ودرجة حرارة التشبع للحالة النهائية
، جول/كيلوجرام
إذا لم تتوفر بيانات الإنثالبي اللازمة للمعادلة أعلاه، تستخدم المعادلة الآتية:
- X = 100 · cp (Tu – Td) ÷ Hv
حيث: X = نسبة وزن السائل المتبخرة cp = الحرارة النوعية للسائل عند درجة حرارة والضغط الابتدائي جول/كيلوجرام °C Tu = درجة حرارة السائل الابتدائية °C Td = درجة حرارة التشبع °C للسائل عند الضغط النهائي Hv
= درجة حرارة التبخر للسائل عند الضغط ودرجة حرارة التشبع النهاية
جول/كيلوجرام
يستخدم هذا النوع من التبخير الفجائي في تحلية مياه الآبار أو مياه البحار بواسطة التقطير المفاجئ المتعدد المراحل. يسخن الماء ويعاد إلى مرحلة تمدد فجائي بخفض الضغط فجأة، حيث يتحول جزء من الماء إلى بخار. ثم يُكثف البخار مكونا ماء خالي من الأملاح. وتمرر كمية الماء الملحة المتبقية إلى عملية تمدد مفاجئ ثانية عند ضغط أقل من ضغط المرحلة الأولى.
ويستمر تحول كميات من الماء إلى بخار بطريقة التبخير المفاجئ ، ثم تكثف إلى ماء خالي من الملح. وتستخدم الجزء الأكبر من منشآت تحلية المياه على مستوى العالم طريقة التبخير الفجائي المتعددة المراحل. وتتكون تلك المنشآت في العادة من 24 مرحلة متتالية للتبخير الفجائي.
اقرأ أيضا
المراجع
| المزيد من الصور والملفات في كومنز عن: تبخير فجائي |